E aí pessoal! Faz um tempinho que não aparece nada novo nessa blog não é!? :P
Mas para limpar a poeira está aqui um vídeozinho sobre Química Orgânica do nosso parceiro de sempre: O Vestibulando Digital!
Fiquem com Deus!
Mostrando postagens com marcador Postagens com Vídeo. Mostrar todas as postagens
Mostrando postagens com marcador Postagens com Vídeo. Mostrar todas as postagens
quinta-feira, 16 de maio de 2013
quinta-feira, 13 de dezembro de 2012
Energia de ionização
A energia de ionização , também conhecida como potencial de ionização , é a energia mínima necessária para “arrancar” um elétron de um átomo isolado e no estado gasoso, o potencial de ionização é uma propriedade periódica, pois quanto maior o tamanho do átomo ou do raio atômico, ou seja, quanto maior for o número atômico, menor será a energia de ionização, porque os elétrons estarão mais afastados do núcleo e a força de atração entre eles será menor.
Portanto, a variação da energia de ionização na tabela periódica, numa mesma família, aumenta de baixo para cima, e, num mesmo período, da esquerda para a direita,isso é mostrado abaixo, além dos valores das energias de ionização de vários elementos
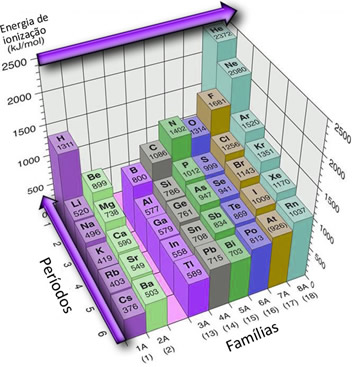
Esse crescimento é inversamente proporcional ao crescimento do raio atômico. É por isso que, conforme visto no texto , o sentido do crescimento dele na Tabela Periódica é exatamente o contrário (de cima para baixo, da direita para a esquerda) do sentido do aumento da energia de ionização.

Vídeos da net: Equação Termoquímica e Energia de Ligação
Boa noite leitores, aqui está mais uma ajuda bem rocheda para vocês! Um vídeo do professor Dino resolvendo uma questão de equação termoquímica e um Aulão do prof. Luis Carlos sobre energia de ligação! Agora o sistema "tá" bruto! Bom proveito!
Fique com Deus!
Entropia
Para medir o grau de desordem de um sistema, foi definida a grandeza termodinâmica entropia, representada pela letra S. Quanto maior a desordem de um sistema, maior a sua entropia.
 |
| Entropia de um corpo negro no universo. |
Os conceitos de processos reversíveis e irreversíveis podem ser descritos matematicamente usando-se o conceito de entropia. Mas antes de chegarmos à definição de entropia, vamos aos conceitos de processos reversíveis e irreversíveis. Chamamos de processo reversível aquele em que o sistema pode, espontaneamente, retornar à situação (ou estado) original. Processo irreversível é aquele cujo sistema não pode, espontaneamente, retornar ao estado original.
Como os conceitos dos tipos de processos já foram citados, vamos então à definição de entropia. A entropia de um sistema (S) é uma medida do seu grau de desorganização. Quanto maior a organização, menor a entropia. A entropia é uma característica do estado termodinâmico, assim como a energia interna, o volume e o número de mols.
 |
| O recipiente 2 tem uma temperatura maior do que a do recipiente 1, logo o seu grau de agitação é maior. |
Pilhas de Daniell
As primeiras aplicações importantes da eletricidade provieram do aperfeiçoamento das pilhas voltaicas originais pelo cientista e professor inglês John Daniell, em 1836.
 |
| John Frederic Daniell (1790-1845) |
Pilhas eletroquímicas são sistemas que produzem corrente contínua e baseiam-se nas diferentes tendências para ceder e receber elétrons das espécies químicas.
A pilha de Daniell é constituída de uma placa de Zinco (Zn) em uma solução de ZnSO4 e uma placa de Cobre (Cu) em uma solução de CuSO4. As duas soluções são ligadas por uma ponte salina, ou por uma parede porosa.
Os Elétrons da Química (Eletroquímica)
 |
| Esta postagem consome menos energia! |
A eletroquímica está muito presente no nosso dia-a-dia. Está presente basicamente em pilhas e baterias utilizadas em aparelhos eletrônicos, como celular, controle remoto, lanternas, filmadoras, calculadoras, brinquedos eletrônicos, rádios à pilha, computadores, e muitos outros.

As reações de oxirredução (oxidação e redução) também estão presentes no cotidiano, como na oxidação do ferro (formação da ferrugem), redução de minérios metálicos para a produção de metais, formação do aço, corrosão de navios, etc.
A conversão de energia elétrica em energia química é um processo não-espontâneo, chamado de eletrólise.

Desenho químico: "Los inventores: Marie Curie ep. 22"
Em português:
Olá mais uma vez, caro frequentador rochedo do nosso blog! Estamos aqui para apresentar a vocês este desenho animado químico, para voltarmos a nossa infância estudando química! Neste episódio de "Los Inventores" (o áudio é em espanhol) vamos ver a história de Marie Curie, responsável por grandes descobertas no campo da radioatividade e pelo descobrimento de dois elementos químicos: O rádio e o polônio. Foi ganhadora de dois prêmios nobéis, sendo um da Física e outro da Química. Aproveitem a animação!!! :D
En español:
Hola de nuevo, queridos roca goer de nuestro blog! Estamos aquí para presentar a ustedes esta química de dibujos animados, para volver a nuestra infancia estudiando química! En este episodio de "Los inventores" (el audio está en español) vemos la historia de Marie Curie, responsable de grandes avances en el campo de la radiactividad y el descubrimiento de dos elementos químicos: el radio y el polonio. Se nobéis ganar dos premios, uno de física y otro para la química. Disfrute de la animación! :D
Olá mais uma vez, caro frequentador rochedo do nosso blog! Estamos aqui para apresentar a vocês este desenho animado químico, para voltarmos a nossa infância estudando química! Neste episódio de "Los Inventores" (o áudio é em espanhol) vamos ver a história de Marie Curie, responsável por grandes descobertas no campo da radioatividade e pelo descobrimento de dois elementos químicos: O rádio e o polônio. Foi ganhadora de dois prêmios nobéis, sendo um da Física e outro da Química. Aproveitem a animação!!! :D
En español:
Hola de nuevo, queridos roca goer de nuestro blog! Estamos aquí para presentar a ustedes esta química de dibujos animados, para volver a nuestra infancia estudiando química! En este episodio de "Los inventores" (el audio está en español) vemos la historia de Marie Curie, responsable de grandes avances en el campo de la radiactividad y el descubrimiento de dos elementos químicos: el radio y el polonio. Se nobéis ganar dos premios, uno de física y otro para la química. Disfrute de la animación! :D
Casos particulares das entalpias: Energia de Ligação

 Quando ocorrem reações químicas, ocorre também quebra das ligações
existentes nos reagentes, mas novas ligações são formadas nos produtos.
Esse processo envolve o estudo da variação de energia que permite
determinar a variação de entalpia das reações.
Quando ocorrem reações químicas, ocorre também quebra das ligações
existentes nos reagentes, mas novas ligações são formadas nos produtos.
Esse processo envolve o estudo da variação de energia que permite
determinar a variação de entalpia das reações. O fornecimento de energia permite a quebra de ligação dos reagentes, esse processo é endotérmico, mas à medida que as ligações entre os produtos se formam o processo muda: fica exotérmico. Por quê? Ocorre a liberação de energia.
A energia liberada na formação de uma ligação é numericamente igual à energia absorvida na quebra desta ligação, portanto a energia de ligação é definida para a quebra de ligações..
Resumindo: É a energia necessária para romper um mol de ligação química de uma substância no estado gasoso, a 25 ºC e 1 atm
- Execício resolvido
quinta-feira, 29 de novembro de 2012
Dica de Termoquímica
Bom gente no vídeo você irá ver uma resumida explicação do Prof. Dino sobre termoquímica com cálculos e resoluções na variação de energia e variação de entalpia...
Esperamos ter ajudado..
Bons estudos!!!
quinta-feira, 8 de novembro de 2012
Música dos elementos
Olá meus caros rochedos e rochedas! Estamos disponibilizando no blog de química mais rochedo do Brasil (Exagerei, mas ainda chegamos lá!) o hit químico mais pop do momento! Composto por Tom Lehrer, este é o "The elements" para aqueles que querem treinar o seu inglês e acrescentar um certo conhecimento sobre tabela periódica no seu repertório epistemológico. Bom proveito!
Isso é tudo pessoal!
Fiquem com Deus!
quinta-feira, 12 de julho de 2012
Experimento: Conceito de reagente limitante
Abaixo mais um vídeo em espanhol para 'ustedes'! O vídeo mostra um experimento que introduz o conceito de reagente em falta (ou reagente limitante) e o de reagente em excesso. Assunto de uma de nossas postagens da série casos especiais de estequiometria. Bom proveito!
Clique abaixo para ir ao vídeo!
Clique abaixo para ir ao vídeo!
segunda-feira, 18 de junho de 2012
Casos particulares de Estequiometria (Parte IV): Quando os reagentes são substancias impuras
Até o momento vinhamos trabalhando com substâncias puras (100%) , que têm custo mais elevado porque são dificilmente encontradas na natureza ou porque passaram por um tratamento de remoção das impurezas. Na prática substâncias desse nível são utilizadas na produção de medicamentos ou em análises químicas muito especiais. É muito comum o uso de reagentes impuros, principalmente em reações industriais, pois, como de certa forma já falado antes, são mais baratos e porque já são encontrados na natureza acompanhados de impurezas (o que ocorre, por exemplo, com os minérios).
Exemplos de casos de substâncias impuras:
Exemplos de casos de substâncias impuras:
 |
| Calcário(CaO) com cristais de pirita (FeS2, também conhecido como ouro dos tolos) |
 |
| Ouro (Au) encontrado na natureza. |
 |
| Calcita (CaCO3) com impurezas |
domingo, 17 de junho de 2012
Sem problemas... Aqui é só solução!
Olá caro leitor rochedo, seus problemas em química acabaram... Vamos publicar aqui só soluções:
 Eta solução! Eta solução! Cuidado ai, chefe! :/ |

É bom pedir desculpa aos leitores
|
sexta-feira, 8 de junho de 2012
Vídeo "Vestibulando digital": Soluções Quimicas
A pedidos do Felipe Santos, está aí postada uma aula de Soluções Químicas, espero que aprendam esse assunto.
sábado, 2 de junho de 2012
Animação Química: "Este é o oxigênio"
 |
| Oxigênio tentando interagir com o Hélio, porém sem sucesso :( |
Curta de animação 3D: "This is Oxygen"
"This is Oxygen", produzido por Christopher Hendryx no Ringling College of Art + Design como tese para o departamento de Informática e Animação.
domingo, 22 de abril de 2012
Experiências com Estequiometria
 Os dois vídeos abaixo mostram o trabalho sério de químicos em laboratório fazendo experimentos que envolvem estequiometria. No primeiro exemplo o trabalho é para determinar a fórmula molecular de um composto, já o segundo vídeo é para mostrar como se determina a massa atômica de um metal. O áudio está em espanhol, mas dá para nós que falamos português entender a aplicação dos cálculos estequiométricos, observar como são feitos os procedimentos corretamente e ficar com aquela vontadezinha de mexer nos equipamentos caros da faculdade.
Os dois vídeos abaixo mostram o trabalho sério de químicos em laboratório fazendo experimentos que envolvem estequiometria. No primeiro exemplo o trabalho é para determinar a fórmula molecular de um composto, já o segundo vídeo é para mostrar como se determina a massa atômica de um metal. O áudio está em espanhol, mas dá para nós que falamos português entender a aplicação dos cálculos estequiométricos, observar como são feitos os procedimentos corretamente e ficar com aquela vontadezinha de mexer nos equipamentos caros da faculdade.
Os vídeos foram muito bem desenvolvidos por alunos de Licenciatura em química da Universidad Complutense de Madrid em 2010.
Determinando a fórmula molecular de um composto.
Determinando a massa atômica de um metal.
Bom dia, boa tarde ou boa noite dependendo do horário em que estiver lendo este post.
Fiquem com Deus!
segunda-feira, 2 de abril de 2012
Cálculos Químicos de forma simplificada
domingo, 1 de abril de 2012
Cálculo de volume estequiométrico
E ai galera que visita o nosso humilde blog, segue abaixo um pequeno vídeo esclarecendo um pouco sobre um assunto que pode lhes confundir nessa área de estequiometria : As CNTPs. Assista o vídeo com atenção e com certeza você poderá até ensinar outras pessoas depois...O vídeo foi desenvolvido pelo Centro de Apoio.com e é apresentado pela linda Professora Tarcilla Passos...Yeah! Bom Estudo!
sábado, 31 de março de 2012
Estequio... o que!?
É estequiometria rapaz! vem do grego στοιχείο (elemento) e μέτρο (medida), chegamos a conclusão lógica que estequiometria nada mais é do que "a medida dos elementos". Quando vamos fazer uma churrasquinho no final de semana com os colegas e pensamos: "quantos quilos de carne devo comprar para alimentar esse povo todo?" ai fazemos uma estimativa de quanto cada pessoa irá comer, um ser humano com necessidades normais come mais ou menos 400 gramas de carne, um "pac-man" come de 1 à 5 kg de carne e uma criança come 200 gramas. Daí fazemos os cálculos e chegamos a uma relação da quantidade de pessoas e da satisfação de cada uma.
 |
| Pac-Man: Popularmente conhecido como come-come, personagem famoso pela sua fome que só acaba no fim do jogo |
 |
| Será que vai dar para todo mundo? |
sexta-feira, 9 de março de 2012
Hit da Estequiometria
Um Clássico da química de composição do professor Tiago, com quase 10 mil acessos no youtube, esse Hit está em nosso blog com na versão legenda e a letra aqui em baixo para você detonar em estequiometria!
Com legenda
Versão Original
Assinar:
Postagens (Atom)








