A energia de ionização , também conhecida como potencial de ionização , é a energia mínima necessária para “arrancar” um elétron de um átomo isolado e no estado gasoso, o potencial de ionização é uma propriedade periódica, pois quanto maior o tamanho do átomo ou do raio atômico, ou seja, quanto maior for o número atômico, menor será a energia de ionização, porque os elétrons estarão mais afastados do núcleo e a força de atração entre eles será menor.
Portanto, a variação da energia de ionização na tabela periódica, numa mesma família, aumenta de baixo para cima, e, num mesmo período, da esquerda para a direita,isso é mostrado abaixo, além dos valores das energias de ionização de vários elementos
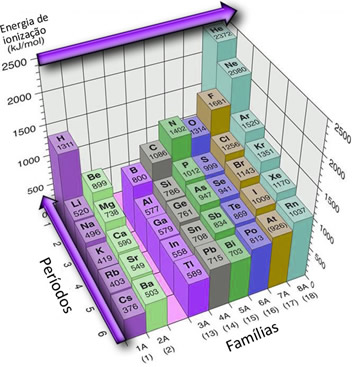
Esse crescimento é inversamente proporcional ao crescimento do raio atômico. É por isso que, conforme visto no texto , o sentido do crescimento dele na Tabela Periódica é exatamente o contrário (de cima para baixo, da direita para a esquerda) do sentido do aumento da energia de ionização.
Outro aspecto importante é que, quando analisamos a primeira e a segunda energia de ionização de um sódio (veja a tabela abaixo), verifica-se que a segunda energia de ionização é sempre maior que a primeira. E a terceira energia de ionização é ainda maior.
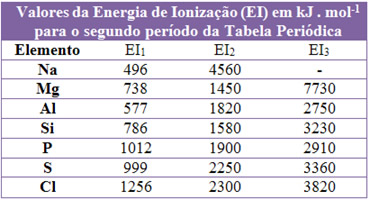
Esse fato ocorre porque quanto mais elétrons se retiram, maior será a atração que o núcleo exercerá sobre os demais elétrons. Consequentemente, haverá um aumento na energia de ionização; ou seja, será necessário fornecer mais energia para romper essa atração com o núcleo.
Por exemplo, considere o caso do magnésio. Como ele pertence à família 2, ele possui dois elétrons na camada de valência. Assim, a energia de ionização para retirar um desses elétrons é 738 kJ . mol-1. Já para retirar o segundo elétron, essa energia aumenta para 1450 kJ . mol-1. Com isso, ele fica com apenas duas camadas ou níveis eletrônicos; portanto, os elétrons estão muito próximos e atraídos ao núcleo. Sua camada de valência agora possui 8 elétrons e para retirar mais um desses elétrons será necessário muito mais energia que na primeira e na segunda energia de ionização (7730 kJ . mol-1). Por esse motivo, o magnésio é encontrado na natureza com a carga +2.
Veja também que as primeiras energias de ionização do fósforo (P), do enxofre (S) e do cloro (Cl) são altas e por isso esses elementos não são encontrados na natureza com carga positiva.
Os ametais possuem energia de ionização alta, porque, assim como os outros elementos representativos, eles têm a tendência de adquirir a configuração eletrônica do gás nobre mais próximo (regra do octeto) e, para isso, eles precisam receber elétrons e não perder, como foi visto neste texto.
Isso é tudo pessoal, obrigado pela atenção, fiquem agora com uma aula de energia de ionização retirada do youtube!!!

Outro aspecto importante é que, quando analisamos a primeira e a segunda energia de ionização de um sódio (veja a tabela abaixo), verifica-se que a segunda energia de ionização é sempre maior que a primeira. E a terceira energia de ionização é ainda maior.

Referências:


Os elementos da tabela são do terceiro período da Tabela Periódica.
ResponderExcluir